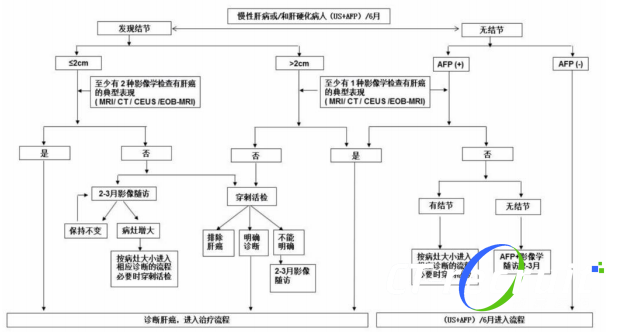
肾癌治疗前沿揭秘:新疗法赋予患者全新希望
肿瘤复发找领募 400-699-8889
据2016年在CA Cancer J Clin上发布的最新癌症统计数据显示:中国大陆肾癌新发病例数为66800例,死亡病例数为23400例,分别位居人群发病率和死亡率的第15位和第17位[2]。
肾癌的发生具有明确的遗传学背景, 约70%肾癌发生的分子基础是VHL基因的缺失、突变导致的基因表达失活。
VHL基因编码一种E3泛素连接酶复合物蛋白,后者可作用于缺氧诱导因子 (hypoxia-inducible factor, HIF) 使之降解。
VHL失活的肾癌细胞内HIF持续活化,从而促进下游一系列靶基因的转录[3]。其中, 下游靶基因血管内皮生长因子 (vascular endothelial growth factor, VEGF) 与血小板衍生生长因子 (platelet-derived growth factor, PDGF) 尤为重要,因为其能够通过与血管内皮细胞上的受体VEGFR或PDGFR结合,促进肿瘤血管生长。
除此之外,PTEN以及TSC1/2等基因失活所引起的PI3K/mTOR信号通路在肾癌发生发展中也十分重要,PI3K/mTOR信号通路调控HIF-α蛋白翻译的重要通路,其在肾癌细胞中持续活化,促进肿瘤血管的生成[4]。
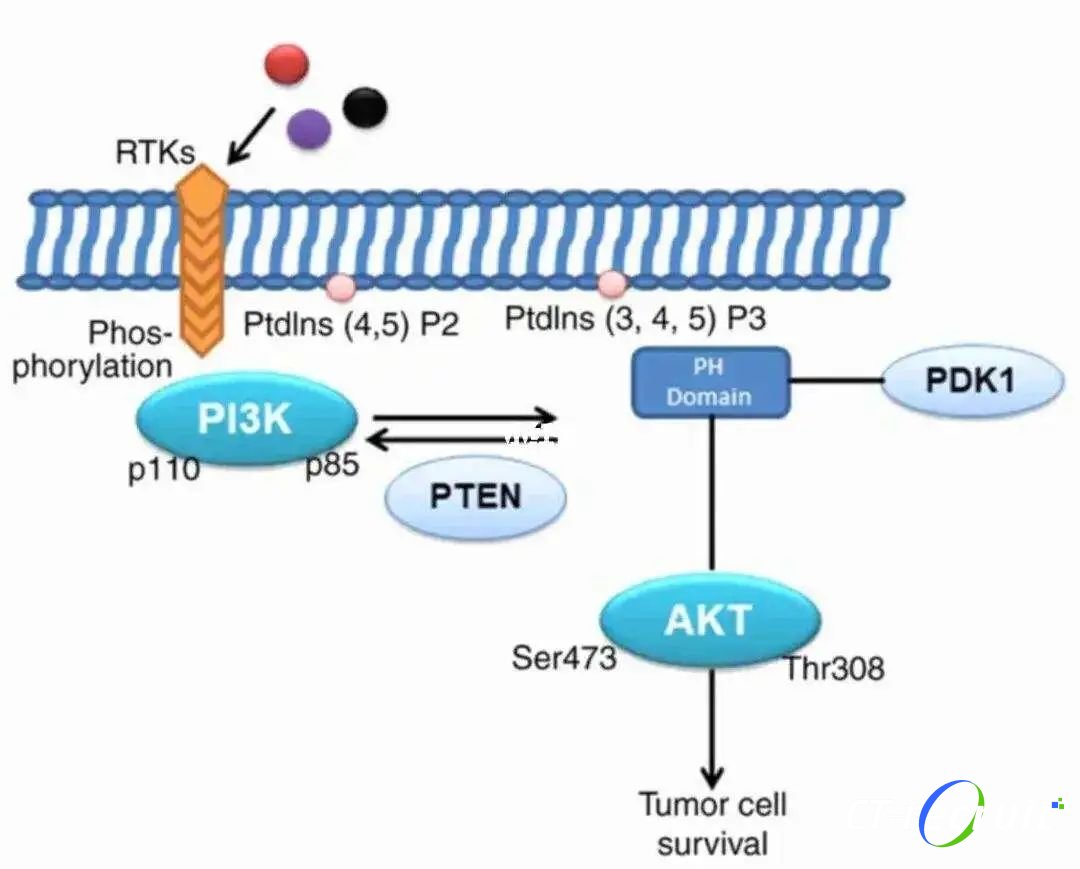
癌肿是单侧还是双侧,是否伴腔静脉瘤栓,是单发还是多发,采取的治疗方法也不同。本文以局限性肾癌的治疗以及转移性肾癌的治疗为切入点,综述不同肾癌的治疗方法。
局限性肾癌的治疗
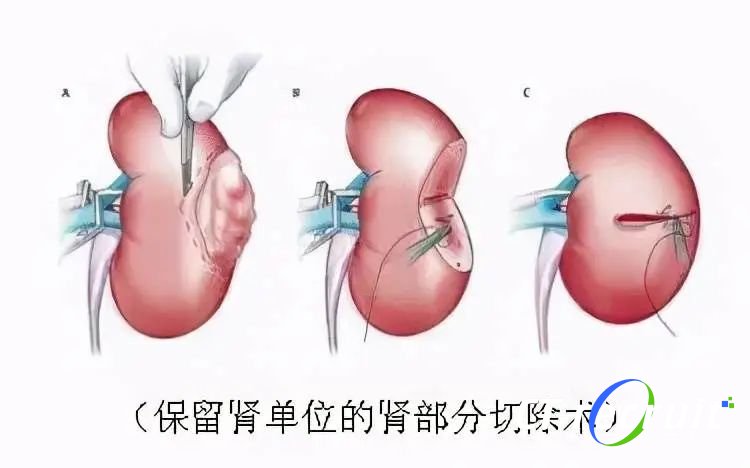
1. 保留肾单位手术 (NSS):
(1)肾部分切除术[6, 7]:对于c T1a期肾脏肿瘤的治疗首选肾部分切除术,可以将CKD或CKD进展的风险降至最低,并且可以获得有利的肿瘤学结果和良好的局部控制。
有证据证明,肾部分切除可以获得根治性肾切除相似的肿瘤学结果。对于复杂囊性肾肿瘤、解剖性或功能性孤立肾肿瘤、双侧肾肿瘤、家族性肾癌或预先存在的CKD或蛋白尿肾肿瘤患者,应优先考虑肾部分切除术。
对于年轻的、多发性肾肿瘤或者患有将来可能导致肾功能不全的伴发病 (如中重度高血压、糖尿病、复发性泌尿系结石、病态的肥胖等) 以及复杂性囊性肾肿瘤患者,应优先考虑肾部分切除术。

在肾部分切除术中,医生应通过尽可能地保留正常的肾单位和缩短热缺血时间,来最大限度地保护肾功能。
术中应尽量做到手术切缘阴性,肾组织切除的范围由手术医生根据患者病情、肿瘤的特性和正常组织界限的判断来决定。
(2)肾肿瘤的剜除术[8, 9]:
对于家族性肾癌、多发性病变、重度CKD患者,以及一些均匀的、包膜完整的肾肿瘤,可以考虑肿瘤剜除术,以最大程度地保留肾单位。
但是在单发肿瘤中如何选择剜除术的标准还没有确定,这需要更多的前瞻性研究进一步加以验证。
2. 根治性肾切除术[10, 11]:当肾肿瘤直径、活检结果结合影像学特征提示肿瘤恶性程度较高时,或愿意积极治疗的患者,应考虑行根治性肾切除术。
凡符合下述所有标准者,则首选根治性肾切除术:
(1)肿瘤解剖学评分高度复杂,即使经验丰富的医生也无法控制手术风险;(2)无CKD或蛋白尿的患者;(3)对侧肾功能正常,且e GFR大于45 ml/ (min·1.73 m2) 。除此之外, 如果可行的话, 均应考虑肾部分切除术。
3. 热消融治疗:对于c T1a期患者也可考虑热消融术作为替代性治疗方案。射频消融和冷冻消融治疗都可以作为热消融治疗的选择。
与手术相比热消融可将并发症降至最低,一般首选经皮方式。在进行热消融治疗前应常规行肿瘤穿刺活检以明确病理。以病理诊断指导后期随访。
在行热消融术前, 应与患者及家属进行沟通,具体内容包括如下:(1)相比外科切除来说首次消融术后肿瘤残留或局部复发的可能性要高;(2)热消融术后可能再次干预治疗。

图片源自网络
转移性肾癌的治疗
1. 细胞因子疗法:转移性肾癌是一种预后不良且对放射治疗和化学治疗均不敏感的肿瘤。
在上世纪,以细胞因子为基础的非特异性免疫治疗一直是转移性肾癌全身治疗的主要手段。
虽然多种细胞因子被证明能抵抗肾癌细胞生长,但仅白细胞介素-2(interleukin-2,IL-2)和 IFN-α 两种细胞因子在临床中疗效最稳定,应用最广泛[12-14]。
 图片源自网络
图片源自网络
2. 抗肿瘤血管生成药物:
(1)索拉非尼:索拉非尼是最早上市用于转移性肾癌的多靶点TKI,除了能通过阻止 VEGF 和 PDGF 与其受体结合阻断血管生成通路外,还可以通过RAF/MEK/ERK 信号传导通路直接阻滞肿瘤细胞生长[15, 16]。
但是由于将索拉非尼作为一线治疗缺乏有效的大型研究结果支持,且替代药物越来越多,目前美国国家综合癌症网络(NCCN)指南及 EAU 指南均未推荐将索拉非尼作为转移性肾透明细胞癌的一线药物,而更愿将其推荐为一线治疗失败后的后续治疗。
(2)舒尼替尼:舒尼替尼靶点与索拉非尼类似,是一种口服小分子多靶点 TKI,抗血管形成是其诱导肿瘤细胞凋亡的主要机制[17]。
(3)培唑帕尼:培唑帕尼是一种作用于 VEGFR-1、 VEGFR-2、PDGF受体(PDGF receptor,PDGFR)的多靶点 TKI。
且基于目前的临床试验结果,NCCN 及 EAU 指南均将培唑帕尼纳入转移性肾癌的一线治疗中,其中, NCCN 指南同时推荐培唑帕尼用于细胞因子治疗后或其他 TKI 治疗后病情进展的患者[18, 19]。
(4)卡博替尼:卡博替尼为作用于 VEGFR-2、肝细胞生长因子受体和 Anexelekto (AXL)的多靶点 TKI,与其他抗血管生成靶向药物不同的是,卡博替尼可阻断肝细胞生长因子信号通路,抑制肿瘤血管再生。
2016年 FDA 批准卡博替尼用于转移性肾癌的二线治疗,现 NCCN 指南推荐卡博替尼为转移性肾透明细胞癌患者二线治疗的首选[20, 21]。
3. mTOR 通路抑制剂:
(1)替西罗莫司:替西罗莫司(CCI-779)可通过与结合蛋白结合形成的复合物来结合 mTOR 的结构域,阻断 mTOR 信号通路,抑制肿瘤细胞增殖、转化及肿瘤血管生成等过程。
已有研究表明,对 MSKCC 分级为高危的转移性肾癌患者或者非透明细胞肾癌患者可从一线替西罗莫司治疗中获益,而对于舒尼替尼一线治疗后病情进展的肾癌患者,VEGF 通路抑制剂索拉非尼优于 mTOR 通路抑制剂替西罗莫司。
NCCN 指南建议,仅针对 MSKCC 分级为高危的转移性肾癌患者,替西罗莫司为I类推荐[22]。
(2)依维莫司:依维莫司为一种口服 mTOR 抑制剂,主要用于舒尼替尼等 VEGFR-TKI 治疗失败后的二线治疗。
但是目前依维莫司二线治疗的地位正在下降,2个大型随机对照试验结果显示在转移性肾癌患者二线治疗中,卡博替尼(METEOR研究)及纳武利尤单抗(CheckMate-025研究)均较依维莫司有更好疗效[20, 23, 24]。
当前肾癌的研究方向主要集中在探明肾癌深层的发病机制、寻找敏感性和灵敏度高的分子、细胞标志物以实现对肾癌的早期监测诊断,同时提供较为可靠的预后信息,进一步探寻新的肾癌的分子靶向治疗、免疫治疗方式。
肾癌诊疗方式多样化的同时,应根据患者具体的病情,综合考虑肾癌的特点,在尊重患者意愿的前提下合理选择诊疗方式。
(向下滑动查看全部)