DS-8201
肿瘤复发找领募,400-699-8889,抗癌路上,能少一丝无奈,多一点希望!
“明星药”DS-8201
抗体偶联药物ADC
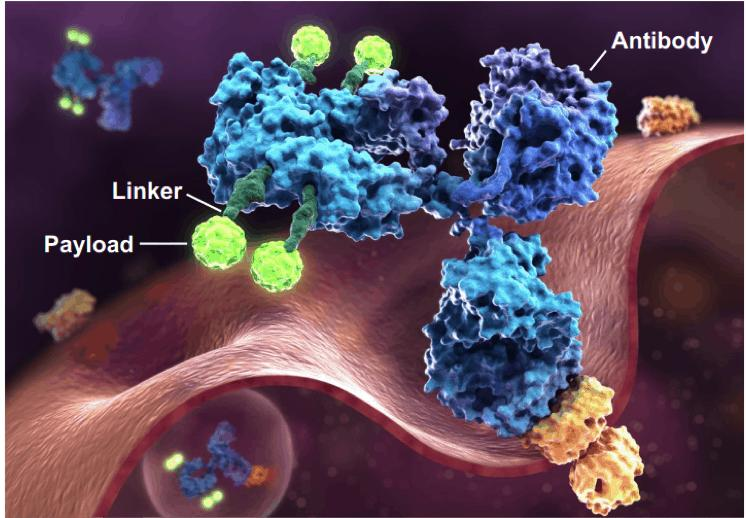
首先需要了解什么是抗体偶联药物?抗体药物偶联药物(antibody-drug conjugate, ADC)是通过一个化学链接将具有生物活性的小分子药物连接到单抗上,单抗作为载体将小分子药物靶向运输到目标细胞中(图1为ADC的示意图)。DS-8201就是这样的连接结构将曲妥珠单抗及德鲁替康用肽基链接在一起。
(图1.ADC的示意图【1】)
绿色椭圆部分为单克隆抗体,蓝色为链接物,黄色圆形为小分子药物。
对于HER-2低表达(IHC1+或IHC2+/ISH-,判定HER-2表达情况见图3)先前接受过充分治疗的这部分乳腺癌患者,54例患者入组后接受至少1剂量的T-DXd,客观缓解率达37%【5】。
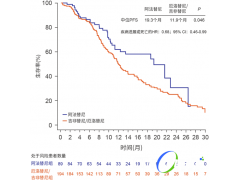
在DS-8201治疗乳腺癌的2期临床试验中(DESTINY-Breast 01),184例先前接受过抗Her2治疗的HER2阳性乳腺癌患者接受了推荐剂量DS-8201a(5.4 mg/kg)的治疗,60.9%的患者对治疗有反应,中位随访时间为11.1个月,中位反应时间为14.8个月,中位无进展生存期为16.4个月。DESTINY-Breast 01试验在晚期乳腺癌患者中的优秀表现,奠定了DS-8201获批治疗晚期HER-2阳性乳腺癌的坚实基础【6】,创造了新的Her2阳性乳腺癌治疗格局。
2、Her2阳性胃癌
晚期HER2阳性胃癌患者在抗HER-2治疗失败后,其他治疗选择包括氟尿嘧啶类、铂类、伊立替康、紫杉醇类和免疫检查点抑制剂等,而这些治疗方案延长患者生存时间效果并不突出,临床上急需更优的挽救治疗方案。在晚期HER-2阳性胃癌的1期临床试验中,44例HER-2阳性的胃或胃食管交界癌患者接受了至少一次DS-8201推荐剂量治疗,客观反应率为43.2%,没有发现药物相关的严重不良事件【7】。
在DS-8201治疗胃癌的2期临床试验中(DESTINY-Gastric01),纳入187名之前至少接受过包括曲妥珠单抗在内的两种治疗方案后发生进展的HER2阳性胃癌或胃食管交界处腺癌患者,125分到DS-8201组,62分到化疗组,DS-8201组客观缓解率为51%,而化疗组仅为14%(具有统计学差异,p<0.001);中位OS为12.5个月 vs 8.4个月;主要的不良反应是中性粒细胞减少、贫血以及白细胞计数减少,DS-8201相关的间质性肺病或肺炎【8】。DESTINY-Gastric01试验结果显示,在使用抗HER-2治疗失败后的晚期胃癌患者,DS-8201明显延长晚期胃癌患者生存的生存期,这也是其获批晚期HER2阳性胃癌/胃食管交界处癌症的支撑数据。
3、Her2阳性结肠癌
研究结果表明,在2-3%的结直肠癌患者中发现了HER-2扩增,令Her2阳性结直肠癌患者的抗Her2治疗充满了希望和期待,尽管目前尚未批准HER-2靶向治疗结直肠癌。DS-8201关于结直肠癌的2期临床试验DESTINY-CRC01表明,纳入对象为HER-2表达的转移性结直肠癌患者,并在之前经历过两种或两种以上方案治疗后进展(包括使用过HER-2靶向治疗),其中HER-2阳性组客观缓解率达45.3%,中位随访时间为27.1周【9】。
关于DS-8201的其他临床试验
HER2治疗展望